La solución de Fehling consiste en dos partes, Fehling A y Fehling B. Fehling A consiste en sulfato cúprico acuoso, mientras que Fehling B consiste en tartrato de sodio y potasio acuoso ($\ce{NaK(C4H4O6)}$). El reactivo de Benedict consiste en carbonato de sodio, citrato de sodio ($\ce{Na2(C6H6O7)}$), y sulfato cúprico disuelto en agua. Ahora está bastante claro que la principal diferencia entre los dos reactivos es el agente complejante (citrato en el de Benedict y tartrato en el de Fehling).
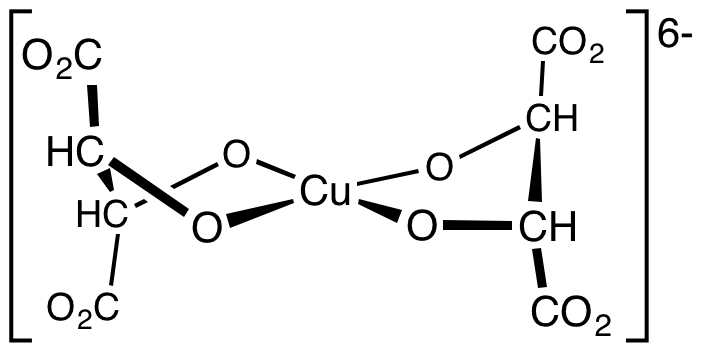
El reactivo de Fehling fue inventado por Hermann von Fehling en 1849. Se nota que esta solución se da como dos soluciones separadas y solo se mezclan durante la realización de una prueba. Esto se debe a que el complejo formado al mezclarlos ($\ce{[Cu(C4O6)2]}$) es cinéticamente favorecido, y que al final $\ce{Cu(OH)2}$ precipitará debido a que es termodinámicamente favorecido. Por eso las dos soluciones se almacenan y solo se mezclan durante el análisis. ![introducir descripción de la imagen aquí]()
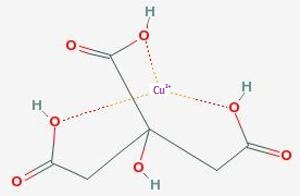
Por otro lado, el reactivo de Benedict fue descubierto por Stanley Rossiter Benedict en algún momento entre 1904 y 1936. Por lo tanto, el reactivo de Benedict se desarrolló después del de Fehling. El complejo de citrato en el reactivo de Benedict es mucho más estable que $\ce{Cu(OH)2}$, por lo que el reactivo de Benedict no precipita al estar mucho tiempo en reposo, a diferencia del de Fehling. Esto es bastante ventajoso ya que no tendría que mezclar dos soluciones para realizar la prueba. Aquí es donde el reactivo de Benedict es muy útil.
![introducir descripción de la imagen aquí]()
Ambos reactivos tienen una forma similar de oxidar aldehídos. El complejo de cobre oxida el aldehído a un ácido carboxílico, y se reduce de $\ce{Cu^2+}$ a $\ce{Cu+}$ ($E^\circ = \pu{0.154 V}$). Este potencial de reducción es suficiente para oxidar aldehídos a ácidos carboxílicos. Sin embargo, aquí no hay mucha diferencia.
Ninguno de los reactivos puede oxidar aldehídos aromáticos, debido a que carecen de α-hidrógenos, y por lo tanto, oxidarlos requiere oxidantes más fuertes (como el reactivo de Tollens).
En resumen, el reactivo de Benedict es como una versión "mejorada" del reactivo de Fehling, que es mucho más estable debido a la diferencia en el agente complejante.