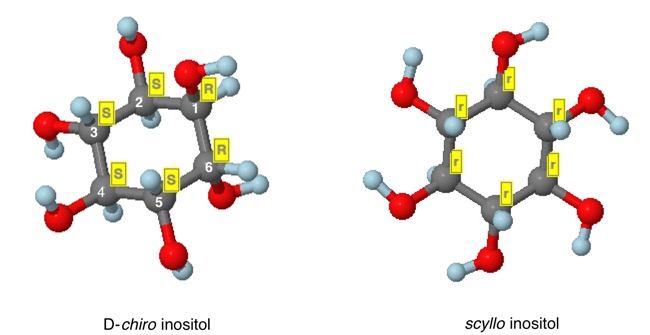
Ofrezco una perspectiva diferente a tu pregunta sobre los inositoles y cómo se determina la quiralidad de los carbonos "superiores" en D-quiro-inositol 2 (C2; configuración S) y escilo-inositol 3 (C2; configuración r).
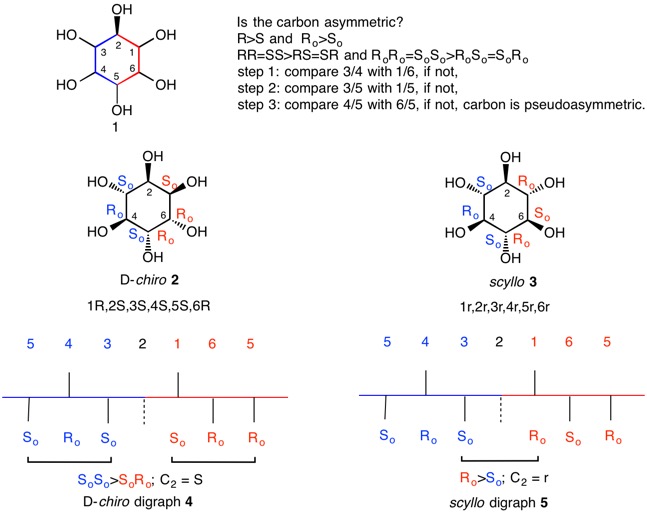
El inositol genérico 1 se numera de la misma manera que D-quiro-inositol y escilo-inositol. Se ilustrará el método para asignar el descriptor CIP para cada inositol en C2. Comenzando desde C2 en la estructura 1, la trayectoria en sentido contrario a las agujas del reloj C2-->C3-->C4-->C5 está coloreada de azul mientras que la trayectoria en sentido de las agujas del reloj C2-->C1-->C6-->C5 está en rojo.
Comenzando con D-quiro-inositol 2, se asignan descriptores temporales (Ro/So) en todos los carbonos excepto en C2. En cada uno de estos carbonos, el grupo hidroxilo tiene la prioridad más alta mientras que el hidrógeno tiene la prioridad más baja. C2 se toma como el grupo de prioridad siguiente más alto, sin importar qué tan lejos esté el carbono en cuestión de C2.1 Las asignaciones temporales para D-quiro-inositol se ilustran en la estructura 2. Para determinar si la trayectoria azul o roja tiene la prioridad más alta, el paso 1 es comparar las asignaciones de C3/C4 (So/Ro) con C1/C6 (So/Ro). En este punto no se puede tomar una decisión. En el paso 2, se compara C3/C5 (So/So) en azul con C1/C5 (So/Ro) en rojo. Porque los descriptores "iguales" (RR o SS) tienen prioridad sobre los descriptores "diferentes" (RS o SR), ya sean temporales o no. Las prioridades para C2 son OH>SoSo>SoRo>H. C2 es de la configuración S. El digrafo 4 también ilustra este punto. Debido a que el D-quiro-inositol es quiral, cada uno de los carbonos es tanto estereogénico como quirotópico. Cada carbono debe ser analizado independientemente como se hizo con C2. Nota que las asignaciones temporales (Ro/So) no tienen relación con las asignaciones finales (R/S). continuar
![ingresar descripción de la imagen aquí]()
![ingresar descripción de la imagen aquí]()
Escilo-inositol 3 es acíclico al tener tres planos de simetría que pasan por C1/C4, C2/C5 y C3/C6. Todos los carbonos son equivalentes; asigna uno, has asignado los seis. Después de asignar descriptores temporales y avanzar hasta el paso 3 (ver reglas al lado de la estructura 1), no se puede tomar una decisión. C2 y todos los demás carbonos son pseudoasimétricos (estereogénicos y acirotópicos). La posición por defecto es usar las asignaciones temporales en C1 y C3 (ver digrafo 5). La Regla CIP 5 establece R>S (y Ro>So). Las prioridades para C2 son OH>Ro>So>H. C2 es de la configuración r. Los descriptores en minúsculas r/s se reservan para carbonos pseudoasimétricos.
Los dos inositoles discutidos aquí tienen descriptores que son R/S o r/s. Esto no necesita ser siempre el caso. Por ejemplo, el muco-inositol tiene cuatro carbonos quirotópicos (R/S) y dos carbonos acirotópicos (r/s).
1) Este método es una simplificación de una metodología más compleja.





2 votos
Siete de los nueve inositoles son acíclicos. Cualquier carbono situado en un plano de simetría se encuentra en ambientes acíclicos (r y s). Aquellos carbonos que no se encuentran en un plano de simetría se encuentran en ambientes cíclicos (R y S). Busqué en Google "quiralidad de los inositoles" y encontré esto: ursula.chem.yale.edu/~chem220/chem220js/STUDYAIDS/isomers/...