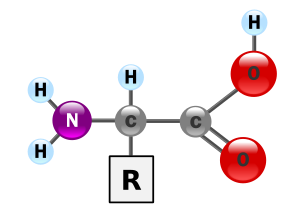
En el sentido más general, el término alfa-aminoácidos no abarcan doblemente sustituidos estructuras como los que usted menciona. Después de todo, el nombre no se especifica ningún sustitución, o la falta de ella, en la α-carbono. El nombre en realidad sólo significa que hay un grupo amino α a un ácido carboxílico, es decir, un carbono de distancia. Similar a la nomenclatura utilizada para describir moléculas donde el grupo amino es de 2, 3, ... carbones lejos de ácido carboxílico, también sin ninguna especificación de sustitución.
![alpha and beta amino acids]()
Los compuestos disustituidos usted la describe, $\ce{H2N-C(R)(R')-COOH}$, pueden ser sintetizados en el laboratorio. Las compañías farmacéuticas parecen tener un interés en estos compuestos. Aquí está un ejemplo de una colaboración entre Eli Lilly y IUPUI1 (hay muchos más - las compañías farmacéuticas como Pfizer,2 incluso tienen algunos de patentes sobre estos compuestos):
![Synthesis of disubstituted alpha-amino acids]()
Wikipedia tiene realmente un ejemplo de un ocurren naturalmente α-amino acid sin un hidrógeno en la α-carbono. Al parecer, es producida por ciertos hongos:
![aminoisobutyric acid]()
Sin embargo, el término alfa-aminoácido es casi siempre utilizado para referirse a la proteinogenic aminoácidos, lo que sucede que tiene un hidrógeno en la α-carbono.
Estos proteinogenic aminoácidos fueron descubiertos hace muchos años. En general, se obtienen por tratamiento de proteínas con ácido (que hidroliza las proteínas en sus aminoácidos constituyentes). Sus fórmulas químicas fueron cuidadosamente identificado por una serie de reacciones de descomposición - de vuelta en los viejos días, no había RMN. La historia del descubrimiento de la proteinogenic aminoácidos se describe en un artículo de revisión3 de 1931(!) - que le dice cuánto tiempo hace que estos fueron descubiertos.
Así, parte de la razón por la que estos no son disustituido es simplemente porque nos pareció que no sea así. Sin embargo, puedo entender si uno se queja de esta conclusión se intelectualmente insatisfactorio. Por lo tanto, aquí es algo más de la especulación.
Uno de los principales pasos implicados en la biosíntesis de los aminoácidos es la transaminación. No tengo una lista conmigo ahora, pero creo que la mayoría de los aminoácidos ir a través de un paso en un momento en el tiempo.
![transamination process]()
El mecanismo descrito en la Wikipedia, o en cualquier libro de texto de bioquímica), requiere que uno de hidrógeno se agrega a la α-carbono. [Para los químicos orgánicos por ahí, este es, esencialmente, una enzima mediada por aminación reductiva.]
Resulta que, en la parte superior de esto, también es posible que tales disustituidos aminoácidos son realmente perjudiciales. De acuerdo a Weber y Miller, escribiendo en el Diario de la Evolución Molecular:4
Reemplazo de la α-hidrógeno por un mayor sustituyente, tales como un grupo metilo, también aumentaría significativamente el impedimento estérico alrededor de los grupos amino y carboxilo. Estérico se han encontrado dificultades en la síntesis química de péptidos con α-ácido aminoisobutírico.
Además, el limitado gravemente estereoquímica comportamiento de los péptidos de la alfa-metil-alfa-amino-n-butírico sugiere que los péptidos compuesto de la alfa-metil aminoácidos sustituidos no habría estructural de la versatilidad de los péptidos derivados de la α-hidrógeno aminoácidos sustituidos.
Un factor adicional que implica la ribosomal de la peptidil transferasa, que sería la de desarrollar una especificidad, ya sea para una α-hidrógeno o un alfa-metil de los aminoácidos. Esto impide la síntesis de las proteínas que contienen ambos tipos de aminoácidos.
Referencias
Verde, J. E.; Bender, D. M.; Jackson, S.; O'Donnell, M. J.; McCarthy, J. R. Mitsunobu Aproximación a la Síntesis de Ópticamente Activos α,α-Disustituidos Aminoácidos. Org. Lett. De 2009, 11 (4), 807-810. DOI: 10.1021/ol802325h.
Graham, S. R.; Mantell, S. J.; Rawson, D. J.; Schwarz, J. B. (Pfizer, Inc.) Derivados de aminoácidos. Patentes de Estados Unidos 7612226 B2, 3 de Noviembre de 2009.
Vickery, H. B.; Schmidt, C. L. A. La Historia del Descubrimiento de los Aminoácidos. Chem. Modif. de 1931, 9 (2), 169-318. DOI: 10.1021/cr60033a001.
Weber, A. L.; Miller, S. L. Razones para la aparición de los veinte codifica para una proteína aminoácidos. J. Mol. Evol. 1981, 17 (5), 273-284. DOI: 10.1007/BF01795749.